Cos'è il Glaucoma?
Il glaucoma è una malattia del nervo ottico che rappresenta una delle più frequenti cause di cecità nel mondo (colpisce circa il 2% dei soggetti di età superiore ai 35 anni). La cecità legata al glaucoma si può quasi sempre prevenire purché la malattia sia diagnosticata e curata tempestivamente. Il danno delle fibre del nervo ottico è lento, progressivo ed asintomatico fino agli stadi terminali tanto che il glaucoma viene definito “killer silente”.
La conseguenza della malattia glaucomatosa è la perdita progressiva della visione periferica che procede se non trattato fino alla perdita della visione centrale. L’ipertensione oculare, coadiuvata da altri fattori che aumentano la vulnerabilità dei tessuti, inizia insidiosamente il danneggiamento del nervo ottico. Un certo numero di fibre entra in sofferenza sino ad essere distrutte. Se non viene istituita in tempo la terapia adatta ne consegue una progressiva lesione del nervo ottico (papilla ottica). In questa struttura la escavazione centrale che é presente anche in molti occhi normali va via via sempre più allargandosi a spese del tessuto nervoso normale. Nelle fasi avanzate la papilla ottica appare atrofica e caratteristicamente escavata detta “a pignatta”.
Tale affezione è familiare.
Cosa succede?
Quando fissiamo un oggetto percepiamo l’oggetto fissato insieme a tutto cio’ che lo circonda: l’area di spazio che viene percepita costituisce il campo visivo. L’immagine per essere percepita viene trasmessa dalla retina al cervello tramite il nervo ottico che si puo’ paragonare ad un cavo elettrico contenente milioni di “fili”. Ciascuno di questi “fili” porta le immagini relative ad una parte del campo visivo; tutte insieme queste parti costituiscono l’immagine nella sua interezza. L’aumento della pressione danneggia irreparabilmente questi “fili”. Inizialmente il danno interessa i fili che portano le immagini relative a porzioni periferiche del campo visivo: il paziente continua a vedere l’oggetto che fissa e non si accorge che l’area di spazio che globalmente percepisce si sta riducendo. Da ultimo vengono lesi anche i “fili” che provengono da quell’area della retina con cui si fissano gli oggetti e si ha la riduzione della acuita’ visiva fino alla cecita’ completa.
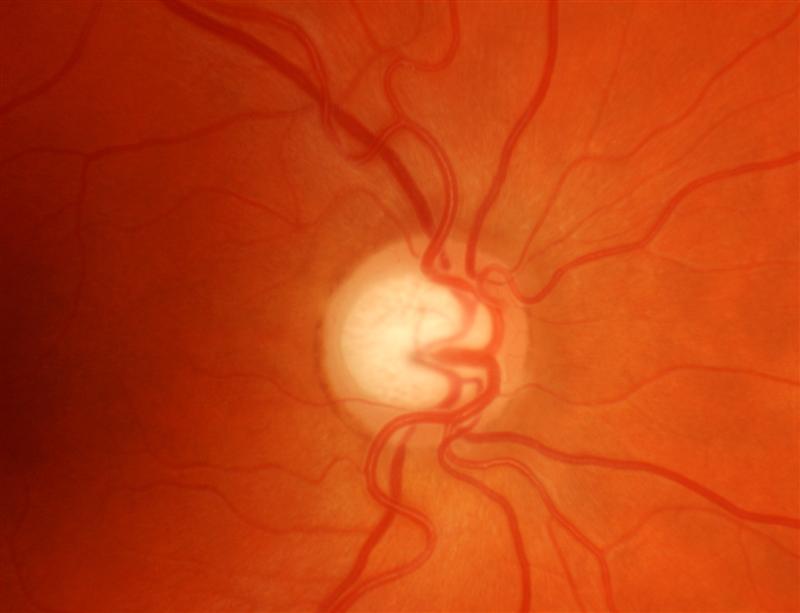
Il nervo ottico
l nervo ottico è il II nervo cranico e trasmette le informazioni visive dalla retina al cervello.
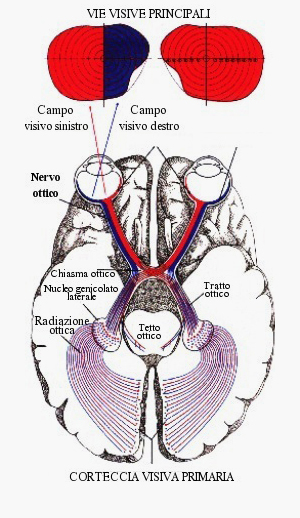
Il nervo ottico dal bulbo oculare lascia l’orbita e attraverso il canale ottico raggiunge il chiasma dove le fibre che lo compongono si incrociano; infatti, le fibre provenienti dalle emiretine nasali si incrociano e proseguono nel tratto ottico controlaterale raggiungendo il mesencefalo la corteccia visiva, area ottica primaria nel lobo occipitale (area 17).
In base ai rapporti che il nervo ottico contrae, il suo decorso è distinto in 4 parti:
- Parte intrabulbare: attraverso membrana coroidea e sclera dell’occhio
- Parte intraorbitaria: dal polo posteriore dell’occhio al foro ottico dello sfenoide
- Parte intracanalicolare: attraverso il foro ottico dello sfenoide
- Parte intracranica: dal foro ottico dello sfenoide giunge al chiasma ottico
Vi sono tre tipi di fibre ottiche:
- Maculari: al chiasma metà fibre incrociano, l’altra metà prosegue diretta
- Nasali: si incrociano totalmente
- Temporali: non incrociano e continuano dirette
Una lesione a carico del nervo ottico produce una perdita permanente dell’acuità visiva.
Prevenzione
Nella maggior parte dei casi la diagnosi di glaucoma viene fatta del tutto casualmente nel corso di una visita effettuata per altri disturbi, o per controllo e non è raro che questa avvenga quando la situazione è già avanzata. Il danno causato dal glaucoma è irreversibile. E’ per questi motivi fondamentale la diagnosi precoce. Tutti gli individui sopra i 40 anni di età dovrebbero sottoporsi ad una visita oculistica una volta l’anno con controllo della pressione oculare e del fundus oculi. In caso di familiarità si consigliano controlli periodici in età più precoce.
Fattori di rischio
La classificazione del glaucoma
L’80% delle forme di glaucoma sono dette ad angolo aperto (glaucoma primario ad angolo aperto) in cui si assiste ad una progressiva degenerazione del nervo ottico in presenza di valori di pressione oculare elevati in assenza di alterazioni anatomiche macroscopiche che possano giustificare tale innalzamento. In percentuale molto inferiore sono i casi di “glaucomi a pressione normale”. In questi casi si assiste ad un progressivo deterioramento del nervo ottico con alterazioni del campo visivo in assenza di valori di pressione oculare elevati. Si ha un glaucoma primario ad angolo aperto ma stretto in cui l’aumento della pressione oculare può essere attribuito alla chiusura anatomica, parziale (glaucoma cronico ad angolo stretto) o totale (attacco di glaucoma acuto), delle vie discarico dell’umore acqueo. Il glaucoma secondario fa invece riferimento a tutte quelle forme di glaucoma in cui è identificabile una causa precisa responsabile dell’aumento della pressione oculare. Tra le numerose forme di glaucoma secondario ricordiamo il glaucoma pseudoesfoliativo, il glaucoma pigmentario, il glaucoma da cortisone, il glaucoma post-traumatico ed il glaucoma neovascolare (spesso associato al diabete o a problematiche vascolari della retina).
L'ipertensione oculare
La pressione normale è in media 16 mmHg. In base a considerazioni statistiche il limite superiore della pressione normale si considera 21 mmHg. La presenza di una pressione intraoculare normale permette il mantenimento della forma del bulbo e il normale funzionamento dei processi fisiologici oculari. Nell’occhio esistono meccanismi di regolazione che tendono a mantenere più o meno costante il limite della pressione intraoculare. Si parla di ipertensione oculare in presenza di valori di pressione oculare superiori a 21-22 mmHg in assenza di danno del nervo ottico o del campo visivo. Chi ha una pressione degli occhi elevata ha un maggior rischio di sviluppare il glaucoma. La decisione di iniziare o meno una terapia va presa d’accordo con il proprio oculista in base alla valutazione completa dei fattori di rischio individua i
Monitoraggio della malattia
Trattandosi di una patologia cronica è fondamentale il monitoraggio della malattia che viene effettuato mediante visite oculistiche periodiche che includono l’esame diretto dell’aspetto del nervo ottico, la misurazione della pressione oculare (tonometria), l’esecuzione di esami computerizzati per lo studio del nervo ottico e delle fibre nervose che lo costituiscono (HRT, GDx, OCT) e l’esame del campo visivo. E’ opportuno sottolineare che la metodica di riferimento per la misurazione della pressione oculare è la tonometria ad applanazione di Goldmann. Altre forme di tonometria (es. tonometria a soffio) non hanno la stessa accuratezza e pertanto non possono essere considerate sostitutive della tonometria ad applanazione. La frequenza delle visite e degli esami può variare notevolmente a seconda delle necessità individuali. Si consiglia l’esecuzione di almeno 6 campi visivi computerizzati nei primi 2 anni dalla diagnosi per inquadrare la velocità con cui la malattia tende a progredire nel singolo paziente, informazione utile a fini prognostici e terapeutici.
La terapiadel glaucoma
Lo scopo della terapia del glaucoma in termini generali è di preservare la funzione visiva del paziente e la relativa qualità di vita. Questo significa rallentare il naturale decorso della malattia ad un livello tale da minimizzare l’impatto della progressione del danno funzionale sulla qualità di vita del singolo paziente. La terapia ipotonizzante oculare, sia essa medica, laser o chirurgica mira a ridurre il rischio di progressione del glaucoma. E’ chiaro a questo punto che la scelta dell’approccio terapeutico deve tener conto delle necessità individuali di ridurre il rischio e rallentare la velocità di progressione e l’aggressività del trattamento (da una efficace monoterapia a terapie d’associazione alla terapia medica massimale fino alla scelta chirirgica) dovrà tenere conto di queste necessità.
La terapia medica si avvale di numerosi principi attivi che usati da soli o in associazione tra di loro permettono di ridurre la pressione oculare o riducendo la produzione di umore acqueo all’interno dell’occhio (beta-bloccanti, alfa-agonisti, inibitori dell’anidrasi carbonica) o favorendone il deflusso (analoghi prostaglandinici, pilocarpina).
La dinamica dell’umore acqueo e la pressione intraoculare dell’occhio glaucomatoso può essere affrontata in quattro modi con terapie topiche (colliri):
- secrezione dell’acqueo (beta-bloccanti, inibitori dell’anidrasi carbonici, alfa2-agonisti)
- deflusso trabecolare (miotici, epinefrina)
- deflusso uveo-sclerale (analoghi delle prostaglandine)
- pressione episclerale venosa/perfusione del corpo ciliare (alfa-2-agonisti con proprietà alfa-1-agonistiche).
La terapia parachirurgica si avvale di laser che vengono impiegati in caso di angolo irido-cornale (angolo di drenaggio) stretto per favorire il deflusso dell’umore acqueo (trabeculoplastica laser) o in caso di angolo di drenaggio stretto per favorirne l’apertura (iridoplastica periferica, iridotomia).
Il laser YAG al neodimio viene usato per praticare iridotomie, indicate nelle forme da chiusura d’angolo.
Il laser ad Argon ed altri laser termici vengono invece impiegati soprattutto per praticare la Trabeculoplastica, indicata nelle forme ad Angolo Aperto e la gonioplastica di uso più raro.
La terapia chirurgica ha comunque lo scopo di ridurre la pressione oculare creando delle vie di deflusso alternative ai liquidi intraoculare.Esistono diverse tecniche chirurgiche, sia penetranti sia non penetranti, con differenti indicazioni in base al tipo di glaucoma. La scelta dipende dall’obiettivo pressorio richiesto, da precedenti trattamenti (farmaci, altra chirurgia), da rischi particolari (per es., soggetto monocolo).La trabeculectomia è l’intervento di scelta nel glaucoma ad angolo aperto. Dopo l’apertura della congiuntiva bulbare, si crea uno sportello sclerale e si asporta un tassello di trabecolato. Lo sportello viene quindi riadagiato, suturato e la congiuntiva richiusa perfettamente. Lo scopo di tale intervento è di creare una fistola ’protetta‘, una nuova via di drenaggio che consenta all’umor acqueo di fluire dalla camera anteriore dell’occhio allo spazio sottocongiuntivale, oltrepassando il trabecolato, la sede dove in questa forma di glaucoma si verifica l’ostacolo al deflusso. Questo processo di filtrazione determina un sollevamento della congiuntiva nella sede chirurgica (bozza filtrante), la cui presenza indica il buon esito dell’intervento. Le complicanze a breve termine includono emorragie, infiammazione della camera anteriore, filtrazione eccessiva con conseguente ipotonia, camera anteriore ridotta o abolita, distacco di coroide. Tra i rischi a lungo termine si sottolineano un’accelerata progressione della cataratta e il rischio di infezione della bozza filtrante, evento che può portare ad un’endoftalmite con potenziali gravi conseguenze per la vista. Nei casi in cui la trabeculectomia ha una bassa probabilità di riuscita si fa uso di impianti drenanti, sistemi valvolari dotati di un tubicino posizionato nella camera anteriore dell’occhio. La sclerectomia profonda è un intervento filtrante non perforante. Questo intervento ha minori complicanze della trabeculectomia. Con questa tecnica la filtrazione dell’umor acqueo dalla camera anteriore allo spazio sottocongiuntivale avviene attraverso una sottile lamella della cornea lasciata in sede. Questa membrana presenta una resistenza al deflusso dell’umore acqueo moderata ma costante, e permette di evitare il brusco calo della pressione intraocular che spesso si osserva in corso di trabeculectomia. Tuttavia i risultati a lungo termine sono spesso inferiori a quelli conseguiti con l’intervento di trabeculectomia.
Nei casi refrattari alla terapia chirurgica convenzionale trovano applicazione gli impianti drenanti o valvole (tipo Baerveldt, Ahmed, Molteno, Express etc.) che prevedono la creazione di una via di drenaggio artificiale dei liquidi intraoculari).
Cheratocono
Cos'è il Cheratocono?
La cornea è una delle lenti più potenti dell’apparato visivo; trasparente, convessa, permette la convergenza delle immagini sul piano retinico. Ha uno spessore “normale” centrale medio di 520-540 µicron e ha una forma ellittica con il diametro maggiore orizzontale lungo 11,7 mm contro i 10,6 mm del diametro minore verticale. Il cheratocono e la degenerazione marginale pellucida sono malattie familiare degenerative della cornea colpiscono uno o entrambi (96%) gli occhi nella maggior parte dei casi in modo asimmetrico. Rare (1 caso ogni 2000 soggetti) ma gravi causano un progressivo calo visivo che inizialmente può apparire come un astigmatismo.
Come già ricorda il nome, si tratta di una deformazione conica della struttura che si allunga dando un’ectasia ed un assottigliamento della stessa all’apice del cono. Questo produce una distorsione delle immagini sul piano retinico.
la patologia si manifesta attorno alla II decade di vita con una evoluzione che nella magior parte dei pazienti continua fino alla V-VI decade perpoi autolimitarsi. Il sesso maschile ha una lieve predominanza (54%).
È una patologia con origine familiare, ma si può presentare in associazione con alcune rare affezioni, incluse alcune malattie allergiche autoimmuni, la sindrome di Down, la sindrome di Ehlers-Danlos, la sindrome di Marfan, la distosi craniofacciale e la osteogenesi imperfetta (tutte condizioni di origine genetica).
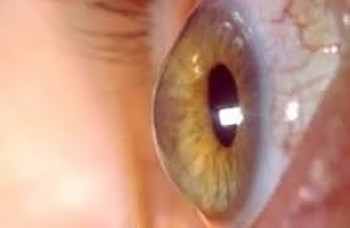
La curvatura irregolare creatasi modifica il potere refrattivo della cornea, producendo distorsioni delle immagini e una visione confusa sia da vicino che da lontano. Il paziente riferisce una progressiva riduzione dell’acuità visiva con comparsa o importante variazione dell’astigmatismo.
Si esegue una valutazione con la lampada a fessura che dimostra, ove già presenti, segni caratteristici della degenerazione conica ed ectasica:
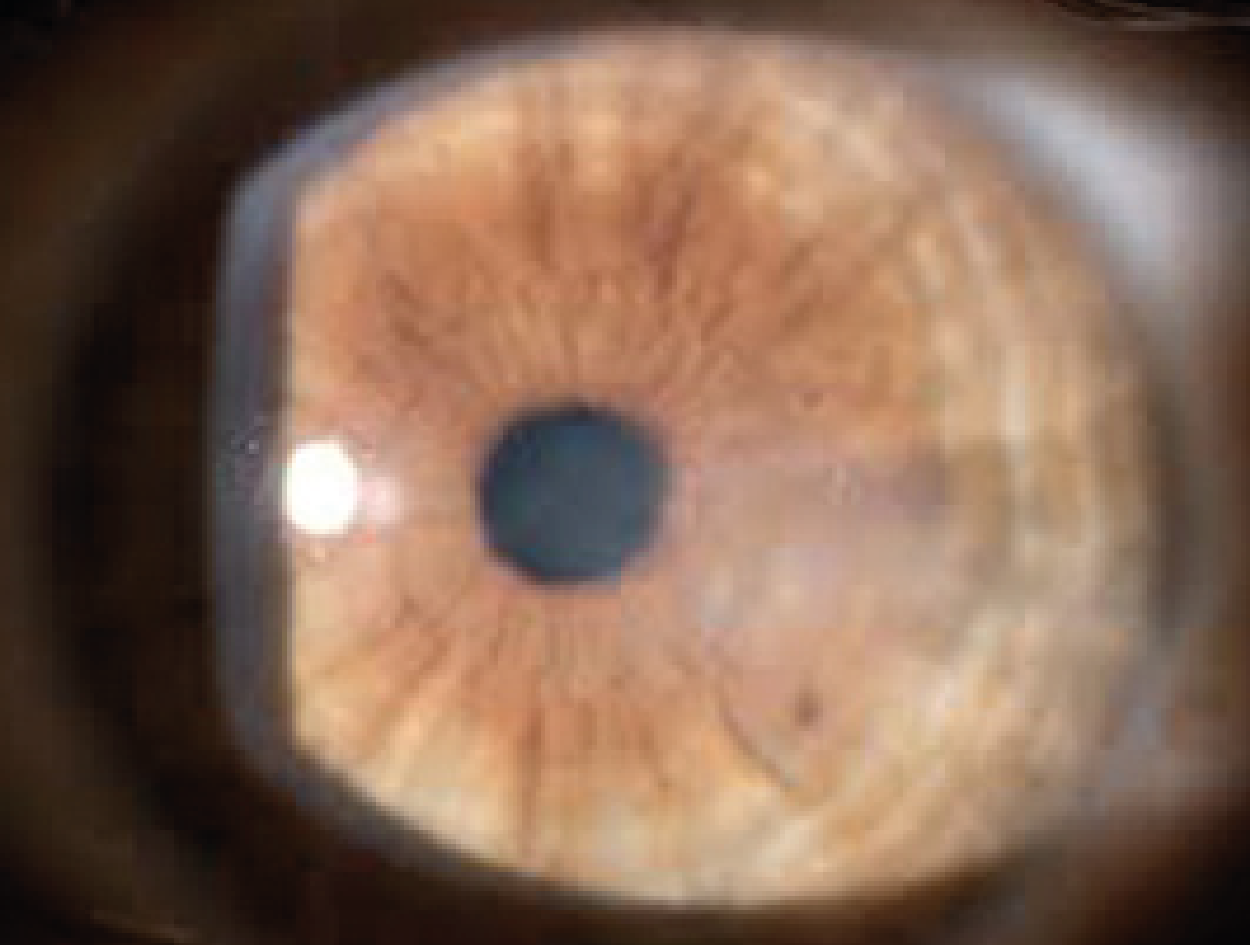
L’anello di Fleischer è un anello giallo-verdastro dovuto all’accumulo di emosiderina nelle cellule epiteliali basali opacità subepiteliali (che si formano da rotture della membrana di Bowman)
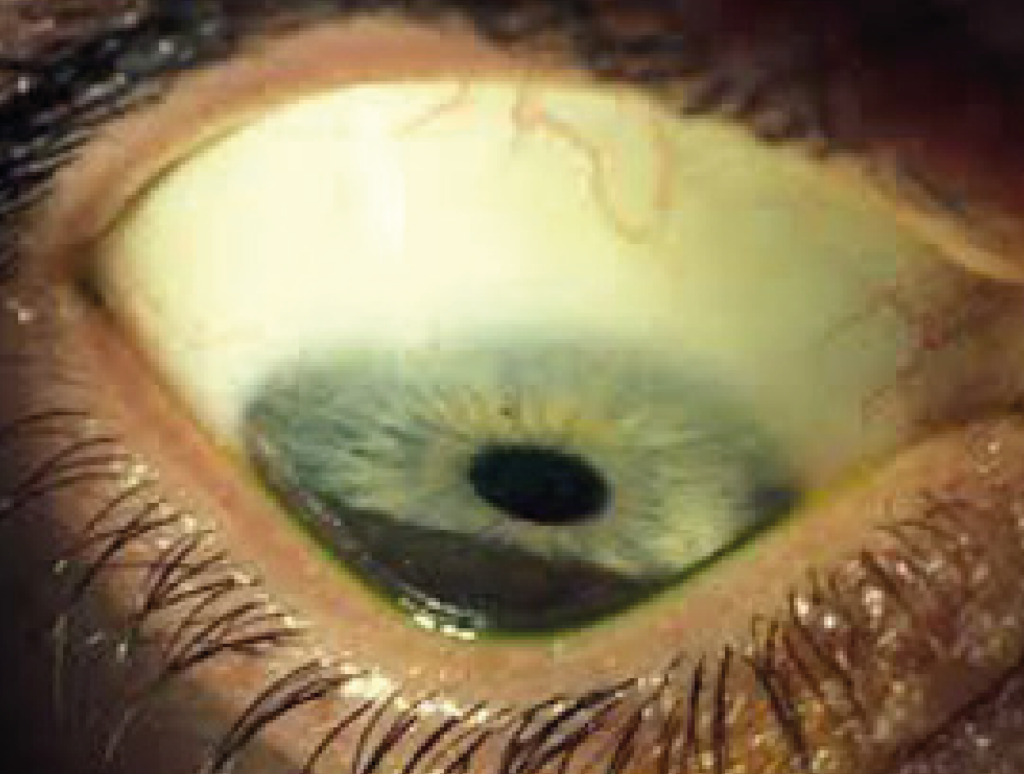
- Assottigliamento stromale maggiore a livello dell’apice del cono,
strie di Vogt
-Segno di Munson, che consiste nella deformazione della rima palpebrale inferiore da parte del cono e si visualizza facendo guardare verso il basso il soggetto
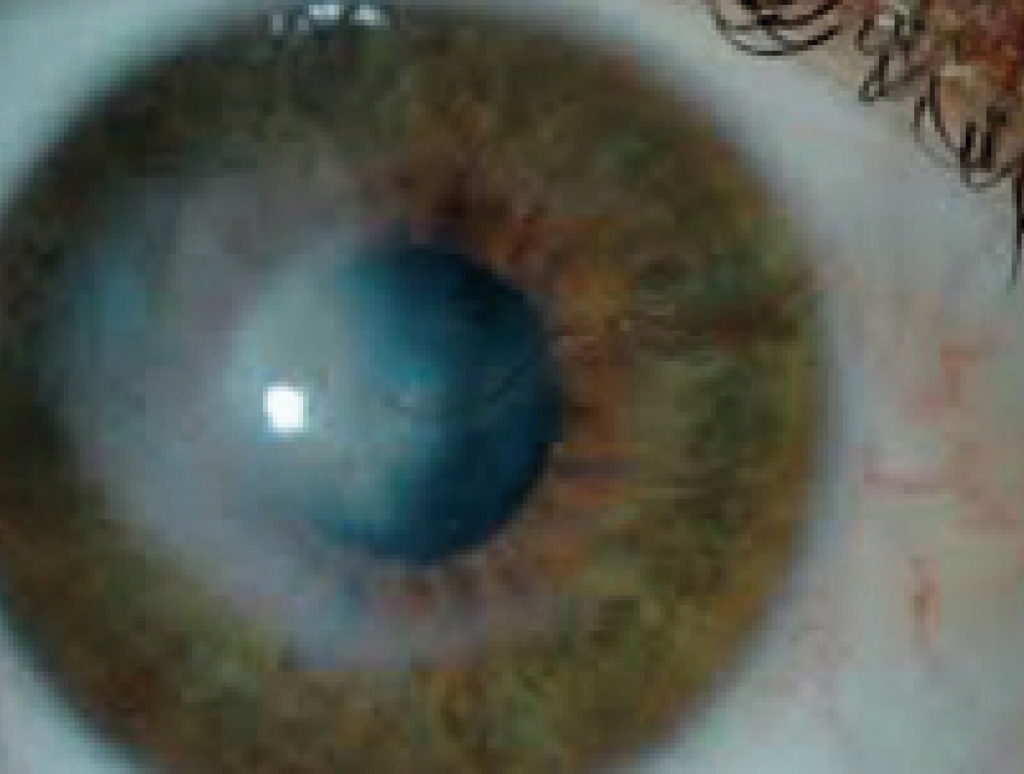
Apice corneale decentrato
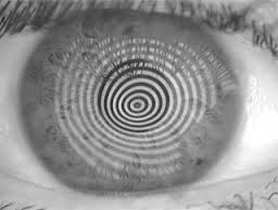
Si esegue un esame oculistico completo con quantificazione dell’acuità visiva “ottimizzata” con lenti.
Si devono eseguire gli esami strumentali specifici quali cheratoscopia (vedi immagine in basso), topografia corneale e pentacam (vedi sezione strumentazione diagnostica)
Stadiazione ed evoluzione
Il cheratocono può essere classificato secondo diversi parametri, a seconda della posizione, della morfologia, della curvatura corneale, dello spessore corneale.
Iniziale
Il cheratocono lieve è caratterizzato da una topografia per la quale ogni punto della mappa è inferiore alle 45 diottrie. Il cono può essere posizionato in qualsiasi parte dell’occhio, anche se è prevalentemente presente nella parte inferiore, leggermente spostato verso la parte nasale.
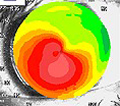
Intermedio
Il cheratocono moderato è caratterizzato da un contorno che si aggira intorno alle 55 diottrie o più. Permangono però delle gradazioni che rappresentano una differenza tra i vari livelli del cono.
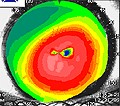
Avanzato
Nel caso del cheratocono avanzato tutto il contorno è superiore alle 55 diottrie. A differenza dell’intermedio, il KC avanzato non ha più differenze di livelli del cono, avendo una colorazione più omogenea che sta ad indicare un innalzamento complessivo.
STADIO – TIPO – DIOTTRIE
I LIEVE <45 D in entrambi i meridiani II MODERATO 45-52 D in entrambi i meridiani III AVANZATO >52 D in entrambi i meridiani
IV SEVERO >62 D in entrambi i meridiani
Stadio Sub-Clinico
Mire: regolari
Visus:10/10 (naturali o corretti)
Raggio Medio: uguale o lievemente inferiore a quello dell’occhio adelfo
Pachimetria: normale o lievemente inferiore
Cheratoscopia: ectasia fuori dalla zona ottica
I Grado
Mire: lievemente deformate
Asse oftalmometrico: obliquo
Raggio Medio: diminuito (in confronto all’altro occhio o a valore precedente)
Visus con occhiali: ridotto
Visus con LAC rigide: ottimo
Topografia: ectasia che interessa la zona ottica
II Grado
Mire: deformate
Raggio Medio: molto diminuito
Asse oftalmometrico: obliquo
Visus con occhiali: molto ridotto
Visus con LAC rigide: buono
Cheratoscopia: ectasia nella zona ottica
Cornea: trasparente/Strie di Vogt, lievemente ectasica
Pachimetria: 0,4-0,45 mm
III Grado
Mire: molto deformate
Raggio Medio: molto diminuito
Asse oftalmometrico: obliquo
Visus con occhiali: < 1/10
Visus con LAC rigide: discreto
Cheratoscopia: ectasia ampia decentrata
Cornea: Strie di Vogt, ectasia evidente, opacità stromali
Pachimetria: 0,35-0,40 mm
IV Grado
Mire: non determinabili
Raggio Medio: non valutabile
Visus con occhiali: < 1/20
Visus con LAC rigide: ridotto
Cheratoscopia: ectasia subtotale e alterata
Cornea: fibrosi apicale, ectasia ben evidente, opacità stromali
Pachimetria: 0,30-0,35 mm
Classificazione morfologica
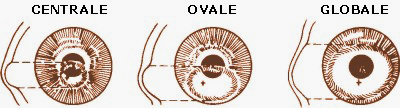
STADIO – TIPO – DIAMETRO
STADIO – TIPO – DIAMETRO
I ROTONDO 5 mm – Cono piccolo circolare
II OVALE > di 5 mm – Cono ovale decentrato
III GLOBALE > di 6 mm – Il cono copre oltre il 75% della cornea
Classificazione basata sulla distanza dell'apice dal centro corneale
TIPO
I Centrale
II Paracentrale
III Periferico
IV Paralimbare (Distrofia Pellucida)
Classificazione di Amsler
GRADO
– I Astigmatismo obliquo con asimmetria delle mire all’oftalmometro di Javal
– II Astigmatismo più elevato con maggiore asimmetria delle mire all’oftalmometro. Assottigliamento evidente in cornea chiara
– III Astigmatismo non misurabile all’oftalmometro di Javal. Assottigliamento corneale marcato
– IV Oltre ai segni precedenti si associa la presenza di opacità corneali lineari
Proprio perché si tratta di una patologia evolutiva e perché i trattamenti “conservativi” possono essere eseguiti se i parametri corneali non arrivano a superare i II-III stadio i pazienti affetti da tale patologia devono sottoporsi a visita oculistica corredata dagli esami topografici e dal pentacam ogni 6 mesi .
Occhiali
Solo negli stadi iniziali o con cheratocono frusto di possiamo prescrivere lenti tempiali ottenendo un buon visus (8-10/10) Con l’evoluzione del cheratocono e l’incremento delle aberrazioni di alto ordine non correggibili con lenti oftalmiche tradizionali, aberrometriche o lenti a contatto morbide “usa e getta” l’unica soluzione è l’uso di lenti a contatto specifiche.
Lenti a contatto Rigide Gas Permeabili per cheratocono
Tali lenti “costruite su misura” per ogni paziente sulla base dei valori della topografia corneale e dell’aberrometria agiscono riducendo l’ectasia corneale dell’apice.
E’ importante che il paziente sia informato che queste lenti riducono sì la degenerazione conica dell’apice, ma non fermano l’evoluzione del cono ed i pazienti devono essere seguiti con controlli periodici al fine di fare diagnosi di evolutività o stabilità dello stesso.
Tali lenti sono state e sono tutt’oggi oggetto di evoluzione sia del materiale di cui sono costitutite sia d nuove geometrie. Può succedere che l’applicazione di lenti a contatto non ha successo in tutti i casi poiché, anche se si riesce a raggiungere un buon visus, a volte non sono ben tollerate e lo scarso comfort non permette di tenere le lenti per un’intera giornata lavorativa.
Il Cross-linking Corneale
Quando la patologia è evolutiva e l’evoluzione è dimostrata dagli esami strumentali il trattamento indicato è il Cross-linking corneale tradizionale o, ultima evoluzione è il cross-liking transepiteliale.
L’obiettivo che si ottiene con questa tecnica è quello di fermare l’evoluzione della patologia “irrobustendo” le fibre di collagene che compongono la cornea che sta sfiancandosi.
La tecnica transepiteliale è relativamente veloce (circa 30 minuti) meno dolorosa nel postoperatorio, in quanto non prevede la rimozione della parte più esterna dell’epitelio.
La tecnica, consiste nell’instillare delle gocce di vitamina B2 (riboflavina) ed esporre la cornea a una luce ultravioletta. La reazione chimica dei raggi UV-A che stimolano la riboflavina comporta un rafforzamento dei legami nel collagene corneale con un conseguente indurimento della cornea.
Il trapianto di cornea o Cheratoplastica
Quando lo stadio del cheratocono è molto evoluto e la cornea presenta gravi alterazioni strutturali che determinano la perdita della trasparenza tanto da ridurre acuità visiva a valori inaccettabili per le normali attività dell’individuo, l’unica soluzione è il trapianto corneale che a seconda della condizione clinica potrà essere lamellare o perforante.
L’intervento consiste nella sostituzione della cornea malata o di una sua parte con quella proveniente da un donatore. Si tratta di un trapianto di tessuto e non d’organo.
Il tessuto corneale è avascolare, cioè non è direttamente nutrito da vasi sanguigni e questo è determinante nello sviluppo della problematica del rigetto che è ovviamente meno frequente
A seconda dello strato corneale compromesso (stroma, endotelio) ci limitiamo al trapianto selettivo del tessuto patologico, lamellare anteriore profondo (DALK – Deep Anterior Lamellar Keratoplasty), in cui viene sostituita la sola porzione anteriore della cornea, senza perforare il bulbo oculare oppure un trapianto di solo endotelio corneale (DSAEK – Descemet Stripping Automated Endothelial Keratoplasty) lasciando intatta la porzione più superficiale sana.
Il trapianto di cornea a tutto spessore (PK o cheratoplastica perforante) viene tuttora riservato a tutti i casi in cui la compromissione corneale è intervenuta a tutti i livelli o ha determinato danni tissutali che non rendono praticabili le altre due tecniche descritte.
Patologie della cornea
Cos'è la cornea?
La cornea è una membrana trasparente, convessa che costituisce la porzione anteriore del bulbo oculare e rappresenta la lente più potente dell’apparato visivo. Assieme al cristallino forma il diottro oculare.
Ha uno spessore “normale” al centro di circa 520-540 µ e, vista anteriormente ha una forma leggermente ellittica con il diametro maggiore orizzontale lungo 11,7 mm contro i 10,6 mm del diametro minore e un diametro variabile dal limbus dov’è più spessa (0,67 mm) alla porzione centrale e più anteriore, la più sottile (0,52 mm).
Anteriormente è a contatto con l’ambiente esterno, le palpebre la proteggono ed il loro ammiccamento permette la distribuzione del film lacrimale prodotto dalle ghiandole lacrimali presenti sulla congiuntiva. Posteriormente è a contatto con l’umore acqueo che riempie e forma la camera anteriore.
Struttura istiologica
La cornea è costituita da cinque strati che dall’esterno all’interno sono:
- Epitelio corneale: pavimentoso composto non cheratinizzato. Consta di 5-6 strati che proteggono la superficie oculare dall’abrasione meccanica e formano una barriera permeabile;
- Membrana di Bowman o lamina elastica anteriore o membrana limitante anteriore: è un denso agglomerato di fibrille collagene;
- Sostanza propria o stroma o parenchima corneale, composta principalmente da fibre collagene. Costituisce la maggior parte della cornea; Tra una lamella e l’altra sono presenti dei caratteristici fibroblasti dalla forma dendritica, i cheratociti, che formano una sorta di rete e maglie larghe tra uno strato lamellare e il successivo. Lo spessore delle fibre collagene tende ad aumentare dalla zona centrale dirigendosi verso il limbo e l’età contribuisce all’ispessimento della cornea.
Gli strati lamellari permettono il passaggio della luce perché le loro fibrille sono più piccole della lunghezza d’onda della radiazione elettromagnetica che le attraversa, inoltre sono precisamente distanziate tra loro e la dispersione è ridotta al minimo dato che le fibrille collagene determinano interferenza distruttiva in tutte le direzioni, tranne in quella anteriore. - Membrana di Descemet o membrana elastica posteriore o membrana limitante posteriore;
- Endotelio: l’endotelio corneale è il quinto e più profondo strato della cornea. Si tratta di un singolo strato di cellule piatte e dalla forma esagonale, con nuclei allungati orizzontalmente. Le sue cellule sono strettamente adese tra loro grazie a interdigitazioni che si dipartono dalle porzioni laterali delle loro membrane plasmatiche, coadiuvate da giunzioni serrate e giunzioni comunicanti. Il loro citoplasma è basofilo a causa dello sviluppo del reticolo endoplasmatico rugoso, possiedono inoltre numerosi mitocondri, risultano cellule ad alta attività metabolica. Il suo compito è essenzialmente quello di fungere da filtro posteriore per gli strati superiori della cornea, è inoltre il principale responsabile della sua idratazione. Le sue cellule hanno una modesta capacità mitotica.
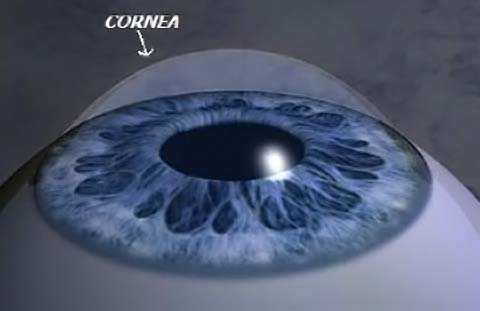
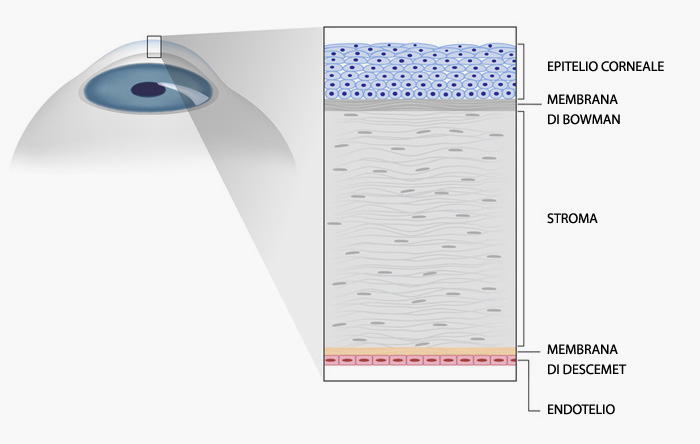
Agli strati precedentemente descritti se ne aggiunge un sesto, lo strato di Dua, di recente scoperta. Questo strato è localizzato nella parte posteriore della cornea, è spesso all’incirca 15 micron e può essere messo in evidenza solo mediante microscopia elettronica, previa insufflazione di aria nello spessore della cornea stessa.
La cornea è avascolare, riceve nutrimento dalle anse vascolari del limbus. Dalla parte interna l’endotelio corneale riceve nutrimento dall’umor acqueo contenuto nella camera anteriore. La cornea è molto innervata con piccoli rami mielinizzati del nervo oftalmico che in parte formano un plesso profondo sopra l’endotelio, in parte attraversano l’endotelio corneale e si proiettano perpendicolarmente nello stroma per poi formare un plesso al di sotto dell’epitelio corneale. Un ultimo plesso sottobasale è costituito da quei piccoli nervi che attraversano la membrana limitante anteriore e si proiettano come terminazioni nervose libere tra le cellule epiteliali; tali assoni presentano caratteristiche espansioni tondeggianti. A partire dall’entrata nello stroma le sottili terminazioni nervose diventano amieliniche. I nervi della cornea sono responsabili dei riflessi dell’ammiccamento e della stimolazione alla produzione del film lacrimale.
La funzione della cornea è quella di permettere il passaggio della luce verso le strutture interne dell’occhio, facendo convergere i raggi luminosi sul piano retinico e per precisione sulla fovea. Il suo potere medio di lente è di circa 43 diottrie, la superficie anteriore (convessa) ha un potere diottrico di +48 diottrie, mentre la faccia interna (concava) ha un potere diottrico di -5 diottrie. La cornea può essere sede di traumi, processi patologici ulcerativi (ulcera corneale), infiammatori (cheratiti), degenerativi (gerontoxon), iperplastico-degenerativi (pterigio), distrofici (cheratocono), tumori benigni o maligni etc. L’opacità corneale è un difetto di trasparenza a seguito di processi degenerativi, cheratiti o ulcere; a seconda del grado di opacamento si distinguono: la nubecola o il leucoma, l’acuità visiva è inversamente proporzionale all’entità dell’opacità corneale ed è tanto minore quanto più centrale è il leucoma. Al potere diottrico totale della cornea contribuisce in gran parte la sua forma, così che modificazioni della normale curvatura della superficie corneale determinano anomalie della focalizzazione delle immagini sulla retina.
Il cheratocono e la degenerazione marginale pellucida sono malattie familiare degenerative della cornea colpiscono uno o entrambi (96%) gli occhi.
Cheratiti
Sezione in aggiornamento.
Patologie della congiuntiva
Cosa sono le patologie della congiuntiva?
La congiuntiva (dal latino coniungo “congiungo”) è la membrana mucosa, sottile, trasparente che tappezza la superficie interna delle palpebre e quella anteriore del bulbo oculare, proprio congiungendole, e appunto per questo è chiamata congiuntiva.
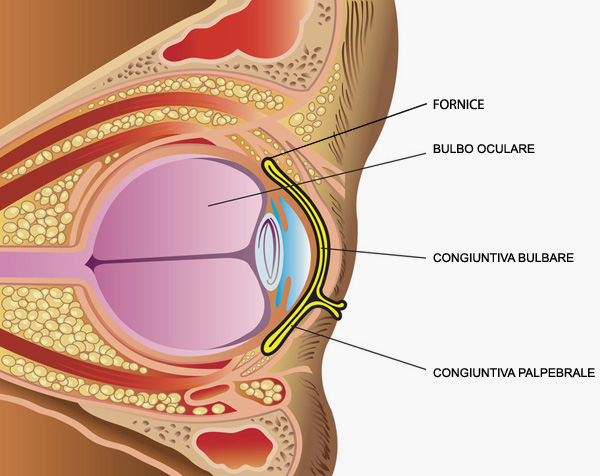
Ne distinguiamo 3 parti anatomiche:
- palpebrale o tarsale
- bulbare
- fornice
La congiuntiva palpebrale aderisce fortemente al tarso (struttura palpebrale sottostante); la congiuntiva bulbare è poco aderente; la congiuntiva dei fornici è abbondante in modo da permettere libertà ai movimenti del bulbo e negli “svuotamenti orbitari” rappresenta il “motore” dell’innesto dermoadiposo che va a ricostruire l’ammanco orbitari.
La congiuntiva è innervata abbondantemente da filamenti del trigemino detti nervi ciliari. Ha una vascolarizzazione complessa, ricevendo propaggini dei vasi palpebrali, dei vasi muscolari e dei vasi ciliari anteriori, nello strato sottocongiuntivale si localizzano ghiandole lacrimali accessorie (Krause e del Ciaccio) e le ghiandole di Henle che producono muco, consentendo lo scorrimento della piega e per far stratificare l’acqua del film lacrimale.
Medialmente la congiuntiva tarsale accoglie i puntini lacrimali superiore ed inferiore che rappresentano la porzione iniziale delle vie lacrimali La principale funzione della congiuntiva è quella di proteggere esternamente il bulbo oculare, grazie al rivestimento che fornisce. Esistono, inoltre, meccanismi di difesa immunitari mediati dal tessuto congiuntivale.
Strutture istologica
È formata da un epitelio di rivestimento e da un tessuto proprio, detto stroma.
L’epitelio è pavimentoso sulla congiuntiva bulbare, cilindrico sulla palpebrale, mentre ha tutti i gradi di passaggio nella congiuntiva dei fornici. Questo epitelio pavimentoso ricorda lontanamente l’epitelio della pelle, e va soggetto come questo a processi infiammatori a focolaio. Il tessuto proprio della congiuntiva è un connettivo, che, specialmente nelle sue parti superficiali, assume i caratteri del tessuto reticolare, o adenoide caratterizzato da larghe maglie e abbondanti leucociti.
Così pure minime sporgenze della congiuntiva palpebrale e dei fornici, possono considerarsi come papille rudimentali. La congiuntiva è ricca di ghiandole mucose e di ghiandoline lacrimali, tutte allo stato rudimentale, fino allo stato di ghiandole unicellulari, quali sembra siano le cellule caliciformi sparse nell’epitelio.
Anche la plica semilunare, rudimento della membrana nittitante, o terza palpebra, che s’osserva in altri animali, e la caruncola lacrimale, che s’osservano al canto interno sono costituite da tessuto congiuntivale.
Le patologie legate alla congiuntiva sono
- Infiammatorie
- Traumatiche
- Cistiche
- Congenite
- Degenerative
- Neoplastiche
Lo pterigio è una patologia della superficie dell’occhio, determinata da una crescita anomala, costituita da un tessuto fibrovascolare, della congiuntiva sulla cornea.
Spesso confusa con lo pterigio, è un accumulo di collagene degenerato localizzato nel settore congiuntivale nasale (ove ha sede anche lo pterigio) e temporale.
Anche la congiuntiva può esprimere neoformazioni benigne o maligne quali degenerazioni delle strutture istologiche che la compongono.
Difetti refrattivi o ametropie
Cosa sono le ametropie?
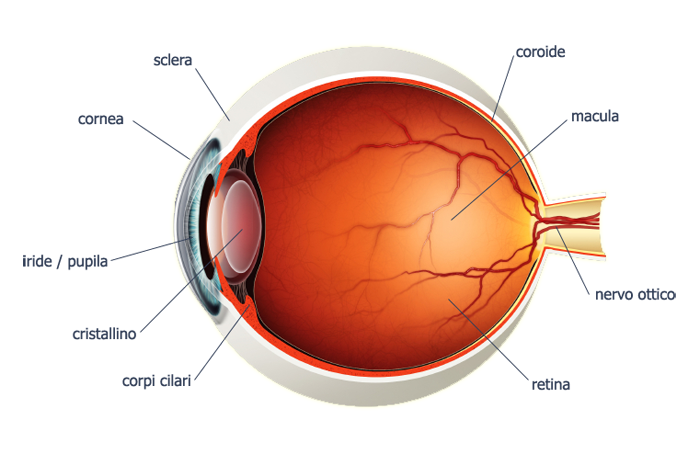
Spesso considerate impropriamente delle malattie, sono dovute, nella maggior parte dei casi, da una imperfetta coincidenza dei rapporti tra curvature corneali e del cristallino (“lenti” dall’elevato potere refrattivo) e lunghezza del bulbo oculare.
Come valutiamo i difetti della refrazione?
La misura della refrazione è l’esame visivo comunemente, e impropriamente, detto “misurazione della vista”. La sua finalità è quella di determinare l’entità del difetto refrattivo e di prescriverne la correzione.
Solitamente, inizia con la determinazione della capacità visiva in termini di acuità visiva (unità di misura sono i decimi).
Quando l’acuità visiva non raggiunge i 10/10 si valuta la presenza di un’ametropia o difetto refrattivo con metodi soggettivi (montatura di prova e lenti o forottero immagine) ed oggettivi ( schiascopia, autorefrattometria e topografia corneale immagine). Se il difetto viene corretto con lenti ottimizzate (unità di misura le diottrie) e non otteniamo comunque la quantità di acuità visiva totale, dobbiamo pensare alle patologie oculari che sono in grado di compromettere questa capacità.
La miopia è un difetto refrattivo o ametropia, nella quale i raggi luminosi provenienti da un oggetto non vengono messi a fuoco sul piano retinico, ma davanti ad esso.
L’astigmatismo è una aberrazione ottica che determina una mancanza di nitidezza visiva a causa di una deformazione della cornea o di un’alterazione delle strutture interne del bulbo.
La presbiopia è una condizione fisiologica dell’apparato visivo, non è un difetto di refrazione, non fa quindi parte delle ametropie.
L’ipermetropia è un difetto refrattivo nel quale i raggi luminosi provenienti da un oggetto non vengono messi a fuoco sul piano retinico, ma dietro ad esso.
L’anisometropia è la condizione in cui i due occhi hanno una diversa refrazione: un occhio è emmetrope e l’altro ametrope, oppure il tipo o il grado di ametropia sono diversi nei due occhi.
L’ambliopia comunemente definita “occhio pigro” è una condizione in cui la funzione visiva di un occhio è ridotta in assenza che ci siano danni oculari organici.